La origino de genetiko
Unu el la plej grandaj misteroj en biologio estas genoj. La genetika kodo estas tiom antikva ke ĉiuj vivantaj organismoj uzas ĝin preskaŭ ekzakte sammaniere. Ĝi estas tiom universala fakte, ke biologoj povas preni genon de unu organismo kaj meti ĝin en tute alian organismon sen multaj problemoj. Ankaŭ la studado de genoj estas antikva. Biologoj kiel Charles Darwin kaj Gregor Mendel detale pristudis heredadon longe antaŭ la malkovro de DNA. Hodiaŭ la genetika kodo estas malĉifrita, sed ankoraŭ ne tute komprenata. Kvankam oni povas analizi la genaron de ajna organismo pli rapide ol iam antaŭe, ankoraŭ restas multaj demandoj: Kiuj genoj faras kion kaj kiel oni eĉ eltrovas tion?
En la 19a jarcento, kiam la pli detala studado de genetiko vere komenciĝis, oni sciis preskaŭ nenion pri ĉeloj. Oni jam delonge povis vidi ĉelojn kaj unuĉelajn organismojn per mikroskopoj, sed multaj pli detalaj strukturoj en la ĉelo simple tro etas por kutima mikroskopo. Por la pioniroj de genetiko, ĉeloj estis nigraj skatoloj kies internaj meĥanismoj simple ne povis esti konataj. Malgraŭ tio, oni sukcesis eltrovi sufiĉe multe pri heredado simple per observado. Charles Darwin estas ĉefe konata pro sia vojaĝado, sed hejme li fanatike bredis kolombojn. Tiel li lernis multe pri kiel la trajtoj de la parencoj influas tiujn de la idoj, kaj finfine li povis klarigi kiel oni kreas novajn variaĵojn de kolomboj per selektado. Alia konata genetikisto estis Gregor Mendel, monaĥo kiu eksperimentis per pizoj. Observante kiel malsamaj trajtoj kiel la koloro de la floro, la formo de la pizo kaj la grandeco de la planto estis transdonataj al la idoj, li sukcesis trovi leĝojn, kiuj regas heredadon.

Laŭ la modelo de Mendel, genoj povas havi malsamajn alelojn. Tiuj estas variaĵoj de la sama geno, kiuj kaŭzas malsamajn trajtojn en la organismo. Por ĉiu geno oni havas du alelojn, kies interagoj difinas kiujn trajtojn oni havas. Ofte unu el la aleloj estas dominanta, kio signifas ke oni nur esprimas la dominantan trajton eĉ se oni havas du malsamajn alelojn. La nedominanta alelo nur esprimiĝas se oni havas du kopiojn de la nedominanta alelo. La trajtoj de la pizoj en la eksperimentoj de Mendel ĉefe herediĝis ĉi tiel. Foje neniu el la aleloj estas dominanta kaj la ido povas esprimi mikson de la du trajtoj, ekzemple kiam purpura kaj blanka floroj produktas rozkoloran idon. En aliaj kazoj, ambaŭ aleloj estas dominantaj kaj esprimiĝas sendepende kaj samtempe. Tio estas la kazo en la sangotipo AB en homoj. Mendel induktis, per sekvado de la heredado de trajtoj, ke gepatroj hazarde transdonas unu el siaj du aleloj al la ido, tiel ke la infanoj havas po du aleloj. Per kalkuli ĉiujn kombinaĵojn, oni povas fari statistikan prognozon pri la aleloj de la idoj kaj per dominanteco oni povas antaŭvidi kiel la trajtoj esprimiĝas.

Historiemuloj foje ŝatas imagi mondon en kiu Darwin estus leginta la laboron de Mendel, sed iliaj teorioj ja iomete frotas. Kaj Darwin kaj Mendel observis bone kaj diligente, sed iliaj konkludoj estis sufiĉe malsamaj. En la modelo de Mendel, aleloj estas kiel fiksaj partikloj. Organismo povas havi malsamajn kombinojn de aleloj, sed la aleloj ne ŝanĝiĝas. En la modelo de Darwin, trajtoj iomete varias en ĉiu ido kaj oni povas draste ŝanĝi specion selektante specifajn trajtojn dum multaj generacioj. Certe ekzistis diferencoj inter la du vidpunktoj, sed malgraŭ tio, ili ambaŭ sorbiĝis de la moderna genetiko. Kiel tio eblas?
La partiklo de genetiko
Je la fino de la 19a jarcento kaj la komenco de 20a jarcento, oni malkovris la materialon kiu enhavas la genetikajn informojn: kromosomoj. Eĉ per la plej bonaj lummikroskopoj, oni kutime ne povas vidi kromosomojn, ĉar ili estas uzataj. Nur kiam ĉelo dividiĝas ĝi kompaktigas la kromosomojn por disigi ilin, kaj tiam ili estas sufiĉe densaj por esti videblaj. Kune kun aliaj genetikistoj, Theodor Boveri montris ke kromosomoj sekvas la leĝojn de Mendel kaj ke ili fakte estas la partikloj, kiuj enhavas la genetikajn informojn. Homoj kutime havas 23 parojn. El tiuj paroj, infano ricevas unu kromosomon de la patrino, kaj unu de la patro. Ili enhavas la samajn genojn, sed ne nepre la samajn alelojn. Tiujn oni heredas ekzakte laŭ la leĝoj de Mendel. La sola escepto estas la sekskromosomoj, kiuj en homoj nomiĝas X kaj Y. Y etas tre malgranda kaj surhavas malmulte da genoj. Tio signifas ke homoj kun la kombino XY havas nur unu alelon de la genoj sur la X-kromosomo, kaj ke nedominantaj trajtoj pli ofte esprimiĝas en tiuj homoj.

Sciante ke kromosomo surhavas multajn genojn, oni povus konkludi ke tiuj trajtoj devus esti ligitaj. En aliaj vortoj, oni ne heredas malsamajn genojn sendepende, sed ricevas ĉiujn genojn sur la sama kromosomo kune. Oni ne malpravus, ĉar genoj ofte herediĝas kune, sed ne ĉiam. La ĉelo havas meĥanismon, per kiu ĝi povas interŝanĝi partojn de la du kromosomoj en paro antaŭ la kreado de seksa ĉelo. Tiel ĝi miksas la alelojn iomete kaj kreskigas la genetikan diversecon de la idoj. La interesa parto de tiu meĥanismo estas ke oni povas uzi ĝin por determini la vicordon de la genoj sur la kromosomo. Por ke unu geno iru al la alia kromosomo kaj la alia ne, tranĉo okazu inter ili. Estas multaj lokoj kie oni povas tranĉi kromosomon, do se la genoj estas tuj apude, la probablo ke la tranĉo okazas inter ili estas malgranda. Tio signifas ke ju pli proksimaj genoj estas sur la kromosomo, des pli ofte ili estas heredataj kune. Se oni kolektas sufiĉe da datumoj, oni povas uzi ilin por kompari la relativajn distancojn inter la genoj kaj finfine krei tutan mapon de la kromosomo.
Konservi informojn en molekuloj
Scienco certe progresis dum la jardekoj kiuj sekvis post la malkovro de kromosomoj, sed oni ankoraŭ ne sciis kiel genetikaj informoj fakte estas konservataj. Tio ŝanĝiĝis ĉirkaŭ la mezo de la jarcento. Oni jam atendis ke la genetikaj informoj estis konservataj en granda molekulo, eble proteino, ĉar grandaj molekuloj estas surprize stabilaj. En 1944, Erwin Schrödinger kreis teorian bazon por subteni tiun supozon. La fiziko malantaŭ lia modelo, kvankam interesa, estas tro detala por ĉi tiu afiŝo, sed la rezultoj ja estis interesaj. Li enkondukis la koncepton de ”neperioda kristalo”. Kutimaj kristaloj konsistas el fiksa unuo de kelkaj molekuloj, atomoj aŭ jonoj, kiuj estas ripetataj en ĉiuj direktoj. Tio ne estas bona bazo por konservi informojn, ĉar ripetado estas la malo de informoj.

Pensi pri informoj en atomoj kaj molekuloj malfacilas, sed havas sencon. Nekonscie oni tuttempe konservas informojn tiel. Se oni skribas sur papero, la informoj konserviĝas en la pozicio de la molekuloj en la inko, aŭ se oni tajpas blogafiŝon, la informoj konserviĝas en elektronoj en la komputilo. Kiam temas pri molekuloj, informoj konserviĝas en neantaŭvidebleco. Por kompreni tion, oni devas pripensi kristalon. Se kristalo estas perfekta, ĝi konsistas el nenio krom ripetoj de la sama baza unuo. Tio signifas ke oni povas preni kristalon kaj tranĉi ĝin en du duonoj sen perdi informojn. Oni povas simple rekonstrui ĝin per kopii la bazan unuon. Laŭ Schrödinger la genetika materialo devus esti tre granda kiel kristalo, sed ĝi ne povus esti simpla ripeto. Eble ĝi povus esti kombino de malsamaj bazaj unuoj, kies sinsekvo enhavas la informojn. Oni scias ke tia molekulo ja enhavus multajn informojn, ĉar se oni duonigus ĝin, oni bezonus la informojn de la alia duono por rekonstrui la ĝustan sinsekvon de unuoj.
Jam kelkajn jarojn post la enkonduko de neperiodaj kristaloj, la vera molekula bazo de genetiko estis malkovriĝis: DNA. La molekulo jam estis konata dum longa tempo, sed oni ne ligis ĝin al heredado. Inspirite de la laboro de Schrödinger, Watson kaj Crick publikigis la unuan artikolon, kiu ĝuste priskribas la strukturon de DNA. Ĝi konsistas el du plektitaj fadenoj, kiuj nomiĝas la duopa helico. La individuaj fadenoj estas faritaj el kvar bazaj unuoj, adenino, timino, guanino kaj citozino (ofte mallongigataj kiel A, T, G kaj C). Tiuj unuoj povas aperi en ajna sinsekvo sen multe ŝanĝi la strukturon kaj ĥemiajn trajtojn de la molekulo. Tio igas ilin perfektaj por la konservado de informoj kiel neperioda kristalo. Kvankam Watson kaj Crick ĉiam ricevis, kaj meritis, multe da estimo, oni iĝas pli kaj pli konscia pri la grava rolo de Rosalind Franklin. Ŝi estis bonega eksperimentisto kaj opiniis ke oni ne publikigu teorian modelon kiam oni ankoraŭ ne havas ĉiujn eksperimentajn rezultojn por pruvi ĝin. Eble Watson kaj Crick tro hastis.

La kodo de DNA
Kiam oni malkovris la strukturon de DNA kaj komencis legi la sinsekvon de la bazoj, oni pensis ke oni trovis la sanktan Gralon. Se oni nur povus malĉifri la genetikan kodon, oni povus legi ĝin kiel manlibron. La vero estis malpli simpla ol atendite.
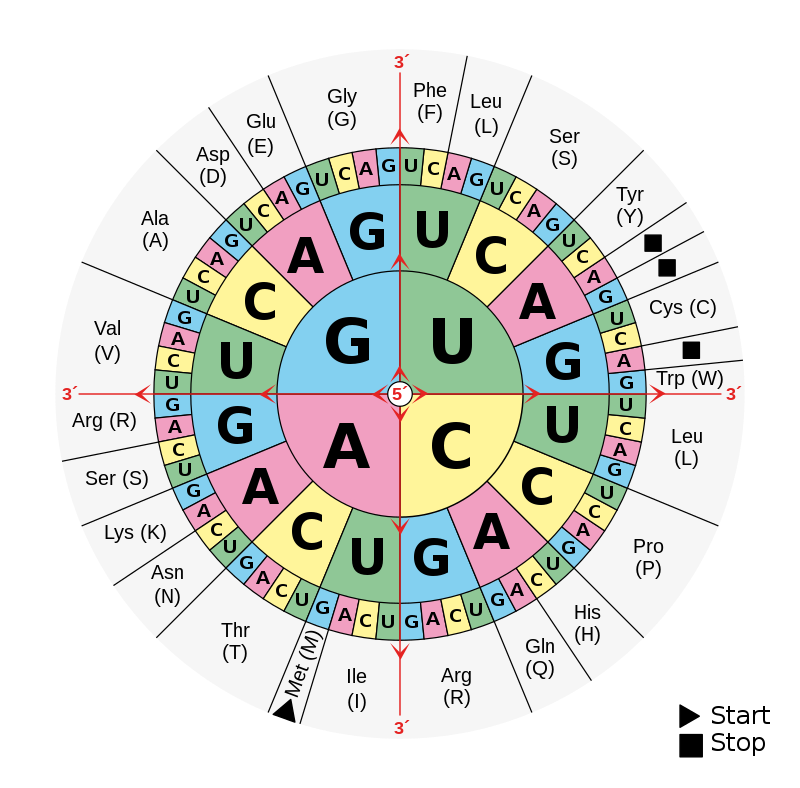
La genetika kodo estis malĉifrita en la 50aj kaj 60aj jaroj per artefaritaj molekuloj de mesaĝa RNA (mRNA). Tio estas unufadena molekulo kiu similas al DNA, sed uzas la literojn A, U, G kaj C (uracilo anstataŭ timino). En la ĉelo ĝi estas uzata por kopii la informojn en la DNA kaj transporti ilin al la proteinfabrikoj: la ribosomoj. Proteinoj konsistas el faldita fadeno de aminacidoj. Tio signifas ke la mRNA devas iel enhavi informojn pri la sinsekvo de tiuj aminacidoj. La plej simpla eksperimento kiun oni povas fari por testi tion estas se oni donas al la ribosomo mRNA-molekulon kiu ripetadas la saman literon, ekzemple UUUUU ktp. En ĉi tiu kazo la rezulto estus fadeno kiu konsistas nur el la aminacido fenilalanino. Tio bonas, sed restas granda problemo. La kodo de la mRNA konsistas el kvar malsamaj literoj, dum proteinoj ĝenerale povas enhavi 20 malsamajn aminacidojn. Alie dirite, oni bezonas plurajn literojn por priskribi unu aminacidon, same kiel 28 literoj povas priskribi ĉiun vorton en Esperanto. Duliteraj kombinoj rezultus je 16 malsamaj ”vortoj”, kio ne sufiĉas. Triliteraj kombinoj rezultas je 64 ”vortoj”, kio estas pli ol sufiĉe. El la restantaj vortoj, tri estas uzataj kiel haltsignaloj, kiuj indikas la finon de la proteino. La aliaj estas uzataj por la samaj aminoacidoj tiel, ke unu aminacido povas esti ĉifrita en 1, 2 aŭ 4 manieroj. Tio protektas la organismon, ĉar tiel ne ĉiu mutacio povas ŝanĝi la proteinon.

Per ŝanĝi la mRNA-molekulojn kaj analizi la produktojn, oni finfine sukcesis krei tabelon por la tuta genetika kodo. La bona novaĵo estas ke tiu kodo estas preskaŭ tute universala, kio signifas ke oni teorie povas igi ajnan organismon esprimi genon de ajna alia organismo. La malbona novaĵo estas ke nur la genetika kodo ne sufiĉas por kompreni organismon. La mRNA priskribas la sinsekvon de la aminoacidoj, sed diras nenion pri kiel proteino faldiĝas aŭ kion ĝi faras en la ĉelo. Nuraj genoj ne diras multe.
DNA en la laboratorio
Por vere kompreni organismon, oni kombinu tion kion oni scias pri la genoj kun tio kion oni scias pri la proteinoj kaj la ĉelo. Hodiaŭ tiaj eksperimentoj ne plu konsistas nur el observado. Sciencistojn havas aliron al multaj teĥnikoj per kiuj ili povas aktive modifi la organismon kaj vidi kio okazas. Se mi volus priskribi ĉiun metodon kiu estas uzata en modernaj laboratorioj, mi bezonus dikan libron, sed mi povas priskribi kelkajn interesajn ekzemplojn.
Antaŭ la komenco de la pandemio, mi ne povis atendi ke PĈR iam enirus ĉiutagajn konversaciojn, sed nun multaj homoj rekte spertis PĈR-bazitan teston. PĈR, aŭ polimeraza ĉen-reakcio, estas metodo por artefarite kopiadi DNA-molekulon, tiel ke oni akiras detekteblan kvanton de DNA, kiu sufiĉe grandas por aliaj eksperimentoj. Ĝi estas rapida kaj efika metodo, ĉar ĝi okazas ekster la ĉelo. La metodo estas bazita sur temperaturŝanĝoj. Se oni plialtigas la temperaturon, la du fadenoj de DNA-molekulo disfalas. Se oni malaltigas la temperaturon denove, la fandenoj trovas unu la alian denove kaj kunfandiĝas. Se oni sukcesus kopii la fadenojn kiam la temperaturo ankoraŭ estas alta, oni povas simple plialtigi kaj malplialtigi la temperaturon en ciklo. La kvanto de DNA-molekuloj ado duobliĝas, ĝis oni havas milionojn da molekuloj en tre mallonga tempo.

La kopiado de DNA okazas per la proteino DNA-polimerazo. Tio estas molekula maŝineto, kiu povas plilongigi unu fadenon de DNA surbaze de la ŝablono sur la alia fadeno. Se oni kreas etajn pecojn de DNA por la komenco kaj la fino de la geno kiun oni volas kopii, la polimerazo povas kopii la genon inter ili. En 1993 Kary Mullis ricevis la Nobelpremion pri ĥemio por enkonduki tiun procezon. Kvankam li certe ŝanĝis biologion por ĉiam, li estas memorata eĉ pli pro siaj frenezaj opinioj. Li opiniis ke scienco estis koruptita kaj li uzis sian famecon por popularigi kontraŭsciencaĵojn kiel la ideo ke aidoso ne rezultas de HIV. Mi povus verki tutan blogafiŝon pri la makulegoj sur lia kariero, sed ĉi tio ne estas klaĉgazeto*.
La plej granda problemo de PĈR estis ke la altaj temperaturoj detruas la DNA-polimerazon. Tio estas malŝparo de materialo, sed eĉ pli de tempo kaj laboro. Por fari PĈR reagon, sciencisto devis aldoni novan polimerazon ĉiun ciklon, dum dekoj da cikloj. La solvo venis de bakterio, Thermus aquaticus, kiu vivas en varma akvo kaj eltenas temperaturojn ĝis 80°C. Pro ĝia ekstrema vivmedio, ĝi havas adaptitan DNA-polimerazon, kiu povas esti uzata je la altaj temperaturoj necesaj por PĈR. Pro tio ke la tiel nomata Taq DNA-polimerazo ne detruiĝas ĉiun ciklon, oni povis vere aŭtomatigi PĈR kaj akiri esence senfine multe da DNA. Hodiaŭ la teĥniko estas uzata en ĉiuspecaj laboratorioj. Oni povas uzi ĝin por detekti malgrandajn kvantojn de virusa RNA (se oni unue konvertas ĝin al DNA), sed ĝi estas aplikata ankaŭ en ekologio, paleontologio, polica laboro kaj tiel plu.
*Por la veraj klaĉemuloj, jen anglalingva superrigardo de ĉiuj klaĉoj:
https://alumni.berkeley.edu/california-magazine/winter-2019/intolerable-genius-berkeleys-most-controversial-nobel-laureate
Legi DNAn
Oni povas kopii DNAn ĝis oni havas plenan tubeton, sed tio nur estas utila se oni povas legi ĝin. Iam tio estis tre malrapida kaj kosta manlaboro, sed hodiaŭ iu ajn povas sendi sian DNAn al entrepreno por analizado. Kiel tio eblas?
Sekvencado, la legado de DNA-sekvenco, komenciĝis en la sepdekaj jaroj. Dum jardekoj la plej populara metodo estis Sanger-sekvencado, kiu ankoraŭ estas uzata por mallongaj pecoj de DNA. La metodo estas bazita sur dudeoksinukleotidoj kiuj fluoreskas. Dudeoksinukleotidoj estas molekuloj kiuj povas ligiĝi al DNA nur je unu flanko, kio signifas ke ili ĉesigas la kreskadon de la ĉeno. Se oni kopias DNA-fadenojn kaj aldonas etan kvanton de tia dudeoksinukleotido, ili estas enmetitaj hazarde, kreante fadenojn de hazardaj longoj. Tion oni faras aparte por ĉiu bazo (A, T, G kaj C). Se oni poste aranĝas la fadenojn laŭ longo (kio eblas per alia teĥniko, kiun mi ne priskribos ĉi tie), oni povas simple legi la literojn de la komenco ĝis la fino. Poste oni inventis maŝinojn por plifaciligi kaj plirapidigi la procezon, kio kaŭzis gradan malkreskon de la kostoj.

La metodo de Sanger estas bona se oni interesiĝas pri specifa peco de DNA, ekzemple por detekti mutaciojn, sed ĝi ne estas taŭga por sekvenci la tutan genaron de organismo. Malgraŭ tio, oni ja sukcesis apliki ĝin por kelkaj genaroj. La unuaj sekvencitaj organismoj estis relative simplaj kiel bakterioj, sed ankaŭ sekvis kelkaj eŭkariotoj, malpli simplaj organismoj kies ĉeloj enhavas ĉelkernon kaj organetojn. La unua estis fornogisto (Saccharomyces cerevisiae) en 1997, kiu havas 16 kromosomojn kun pli ol 12 milionoj da bazparoj kune. Poste venis Caenorhabditis elegans en 1998 kaj Drosophila melanogaster en 2000, du bestoj kiuj gravas kiel modelorganismoj. La unua malneto de la homa genaro estis publikigita en 2001. Ĝi venis ne de unu individuo, sed grupo da anonimaj volontuloj, kiuj donacis sian DNA. Kompreneble oni ne povas legi la tutan homan genaron de pli ol 3 miliardoj da bazparoj en unu fojo, do oni devis esti ruza. Oni dividis la DNA en pecoj de kelkaj centoj da bazparoj kaj sekvencis tiujn, post kio oni kombinis ilin per komputiloj. La rezulto estis malneto pro kelkaj kialoj. Ne ĉiuj homoj samas, do kelkaj partoj de la DNA varias multe, kelkaj partoj estas malfacile kompreneblaj al la komputilo, kaj simple povas okazi eraroj. Dum la sekvintaj jaroj oni ĝisdatigis la malneton.

Saccharomyces cerevisiae 
Caenorhabditis elegans 
Drosophila melanogaster
foton de cerevisiae elegans kaj melanogaster
Se oni hodiaŭ pagas 100 eŭrojn al entrepreno por sekvenco de sia DNA, oni ne igas kompatindan ĥemiiston sekvenci ĉiujn viajn 3 miliardojn da bazparoj per Sanger-sekvencado. Oni ne bezonas sekvenci ĉion. Averaĝe nur milono de la bazparoj estas malsama inter du homoj kaj oni scias ĝenerale kie la interesaj variaĵoj troviĝas. Malgraŭ tio restas ankoraŭ sufiĉe da DNA por sekvenci, do por fari tion necesas modernaj teĥnikoj. Tiuj metodoj nomiĝas Next-Generation Sequencing, aŭ la nova generacio de sekvencado. Mi ne povas priparoli ĉiun individuan metodon ĉi tie, sed la ĝenerala principo estas aŭtomatigo kaj paralela sekvencado. Oni povas meti la DNA-fragmentojn en malsamaj tuboj kaj individue sekvi ilin per la komputilo, tiel ke oni esence faras 100 eksperimentojn samtempe. Pli kaj pli rapida kaj efika softvaro poste kombinas ilin kiel puzlerojn ĝis ĝi trovas la tutan genaron. Hodiaŭ oni trovas respondojn al demandoj pri tutaj organismoj anstataŭ individuaj genoj.
Sekvi proteinojn
La sekvencado de DNA tute ŝanĝis la mondon de genetika eksperimentado. Al Mendel, aleloj estis nevideblaj kaj nur detekteblis per bredado. Hodiaŭ oni povas analizi ies genojn per nenio pli ol tubeto da salivo. Granda diferenco ekzistas tamen inter la ekzisto de iu alelo kaj ties esprimo. Kiel oni scias ke iu geno fakte iĝas proteino? La solvo naĝas en la oceano.
Proteinoj estas tro malgrandaj por kutimaj mikroskopoj, sed oni povas detekti ilin nerekte. Oni povas uzi ekzemple radioaktivajn aŭ fluoreskajn molekulojn, kiuj interagas kun la proteinoj. Unu el la plej sukcesaj ekzemploj de tio estas la verda fluoreska proteino aŭ GFP (Angle: Green Fluorescent protein). Ĝi malkovriĝis en la meduzo Aequorea victoria, kiu produktas bluan lumon kaj uzas GFP por konverti ĝin al verda lumo. Pro tio ke la genetika kodo estas universala, oni povas preni la genon por GFP kaj meti ĝin en kromosomo de tute alia organismo kiel bakterio aŭ insekto senprobleme. Nun GFP estas simpla produkto kiun oni povas fabriki sen meduzoj kaj ĝi estas uzata senĉese en ĉiuspecaj eksperimentoj. Oni eĉ kreis mutaciintajn versiojn kun aliaj koloroj kiel la ruĝan RFP.

Aequorea victoria 
Bakteriaj kolonioj kun malsamaj variaĵoj de GFP
La ĉefa uzo de GFP estas la kontrolado de eksperimentoj. Se oni volas enmeti novan genon en bakterion, oni ne ĉiam scias ĉu oni sukcesas. Oni povas solvi tion per aldoni ankaŭ la genon por GFP. Tiel oni scias ke la fluoreskaj bakterioj enhavas ambaŭ genojn, dum la mallumaj enhavas neniun.
Alia eblo estas la sekvado de proteinoj. Se oni engluas la genon por GFP tuj apud alian genon, oni povas krei hibridan proteinon. Tiajn proteinojn oni povas sekvi en la ĉela per kutima mikroskopo, ĉar oni povas detekti la lumon. Ĉi tiaj eksperimentoj estas gravaj kiam oni volas scii ĉu iu proteino troviĝas ĉefe en la membrano, la nukleo aŭ alia loko en la ĉelo kaj kiel ĝi transportiĝas. Oni estus zorgema tamen, ĉar la aldono de la GFP ne rajtas malhelpi la funkciadon de la ĉefa proteino.
Oni povas sekvi proteinojn ne nur en la ĉelo, sed ankaŭ inter malsamaj ĉeloj. En plurĉelaj organismoj, malsamaj ĉeloj havas malsamajn taskojn kaj fabrikas nur la necesajn proteinojn. Per fluoresko oni povas montri ekzakte kiujn ĉelojn en la korpo esprimas iun genon, specife se la organismo estas travidebla (kiel ekzemple ranido). Pere de tiu metodo, oni povas sekvi kiel specifaj genoj ŝaltiĝas kaj malŝaltiĝas dum la disvolviĝo de besta embrio. Mi povus verki tutan blogartikolon pri tiu temo tamen, do ĉi tiun temon mi konservos por alia fojo 😉

Kaj kio pri la estonteco?
Dum la kolektado de ĉi tiuj informoj iĝis klare al mi, ke la historio de genetiko estas ekstreme riĉa. Unu artikolo neniel sufiĉas por mencii ĉiujn gravajn paŝojn kaj honori ĉiujn sciencistojn, bestojn, plantojn kaj bakteriojn, kiuj kontribuis al ĉi tiu bela kampo. Mi ne povas imagi mondon sen PĈR kaj eĉ malpli mondon en kiu oni ne sciis pri la ekzisto de DNA. Nun la granda demando estas kiel la mondo aspektos post 10, 50 aŭ 100 jaroj. Mi povas esti nur optimisma. Vidante kiel Next-Generation Sequencing disvastiĝis dum mia vivo kaj CRISPR/Cas9 dum la lastaj kelkaj jaroj (kio rezultis je la lastjara nobelpremio pri ĥemio por Emmanuelle Charpentier kaj Jennifer Doudna). Eble ni iam kreos tutan ĉelon en laboratorio.
Plua legado
Interesa anglalingva tempolinio pri la evoluo de sekvencado, kiu estas pli detala ol mi povas esti:
https://www.nature.com/immersive/d42859-020-00099-0/index.html
Licencoj por la bildoj:
Kromosomoj – BaraahAltarayra: https://commons.wikimedia.org/wiki/File:Metaphase5.jpg
Rosalind Franklin – MRC Laboratory of Molecular Biology: https://commons.wikimedia.org/wiki/File:Rosalind_Franklin.jpg
Aparato PĈR – Karl Mumm: https://commons.wikimedia.org/wiki/File:PCR_masina_kasutamine.jpg
Sanger-sekvencado – John Schmidt: https://commons.wikimedia.org/wiki/File:Sequencing.jpg
Saccharomyces cerevisiae – Mogana Das Murtey and Patchamuthu Ramasamy: https://commons.wikimedia.org/wiki/File:Saccharomyces_cerevisiae_SEM.jpg
Caenorhabditis elegans – Kbradnam: https://commons.wikimedia.org/wiki/File:Adult_Caenorhabditis_elegans.jpg
Drosophila melanogaster – Sanjay Acharya: https://commons.wikimedia.org/wiki/File:Drosophila_melanogaster_Proboscis.jpg
Next-Generation Sequencing – Suspencewl: https://commons.wikimedia.org/wiki/File:DNA_Nanoball_sequencing_flow_cell.jpg
Aequorea victoria – Sierra Blakely: https://commons.wikimedia.org/wiki/File:Aequorea4.jpg
Bakteria arto – Nathan Shaner: https://commons.wikimedia.org/wiki/File:FPbeachTsien.jpg
Drozofilo kun GFP – Caitlin Sedwick: https://commons.wikimedia.org/wiki/File:Stage-14_Drosophila_embryo_expressing_AbdA_and_Exd,both_fused_to_one_half_of_the_fluorescent_protein_Venus-_journal.pbio.1001349.g001.png
